Гексацианоферраты металлов обладают ионной и электронной проводимостью, ионообменной способностью, электролитической активностью. На основе этих веществ разрабатывается химические и биологические датчики. В частности, к этим веществам относится берлинская лазурь (БЛ).Несмотря на то, что это вещество известно достаточно давно, поведение его в составе ионоселективных мембран ещё мало изучено.
Композитные мембраны, в состав которых входит порошок смеси графита и БЛ, обладают достаточной эластичностью, минимальным сопротивлением с обеих сторон. Именно БЛ придаёт мембранам ионообменные свойства, т.к. электрод с мембраной на чистом графите дает худший потенциометрический отклик.
Структура БЛ была впервые предложена Кеггеном и Майлсом на основе рентгеноструктурных исследований. Авторы ввели различие между так называемой «растворимой» БЛ KFeIII[FeII(CN)6] и «нерастворимой» БЛ Fe4III[FeII(CN)6]3. Детальное изучение структур гексацианоферратов тяжёлых металлов было проведено Вайзером и др. Атомы железа II и железа III чередуются в узлах гранецентрированной кубической решетки таким образом, что ионы Fe(III) октаедрическио окружены атомами азота, а ионы Fe(II) атомами углерода соответственно. Две трети полостей заполнены атомами Fe(III). Щелочные металлы при внедрении замещают атомы железа в полостях.
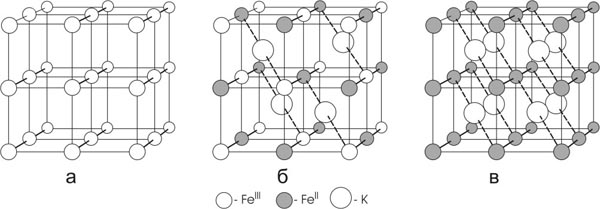
Структура монокристаллов нерастворимой БЛ была исследована в работах Люди с сотр. Она оказалась отличной от структуры предложенной Кеггином. Было отмечено разупорядочивание элементарной ячейки с одной четвертью незанятыми ферроцианидными местами и отсутствие Fe3+ в полостях кристаллической решетки. Таким образом, ферроцианидная решетка обладает отрицательным зарядом, что обуславливает возможность цеолитного перемещения в ней не только положительно заряженных ионов, но и полярных молекул воды, аммиака и др., собственные размеры которых позволяют легко проникать в пустоты решетки.
Электрохимические реакции с участием пленки малорастворимой БЛ, нанесенной на электрод, протекают с участием катионов фонового электролита, которые поступают в плёнку из раствора при её восстановлении и выводятся из неё при окислении.
Участие катионов в окислительно-восстановительных реакциях гексацианоферратов железа делает возможным создание химических сенсоров для неэлектроноактивных ионов.
Гексацианоферрат (II) железа (II) электроактивен в растворах солей цезия, размеры иона которого позволяют ему легко проникать в полости кристаллической решетки берлинской лазури. А ионы лития и натрия блокируют процесс из-за того, что они имеют большой радиус гидратированного иона, что не позволяет им поступать в плёнку.
Существуют многочисленные варианты устройства химических датчиков на основе БЛ. Как правило, это электроды I рода, на который тонким слоем наносятся малорастворимые гексацианоферраты. Известны также модифицированный гексацианоферратом стеклоуглерод, тонкая мембрана ПВХ с включённой смесью графита и гексацианоферрата. Их объединяют следующие требования:
Этим требованиям удовлетворяют плёнки, полученные методом Лэнгмюра-Блоджетт. С его помощью можно нанести тонкий слой вещества (толщиной в несколько молекул) на токопроводящую подложку, подобрав такое ПАВ, чтобы обеспечить минимальное сопротивление мембраны. Преимуществом метода также является возможность контроля состава пленки от слоя к слою при её нанесении.
Состав ПЛБ зависит от многих факторов: строение ПАВ, pH водной субфазы, её ионная сила, двумерное поверхностное давление и др. Следовательно, требуется подобрать такие условия нанесения монослоёв на твёрдую подложку, при которых содержание ионов [Fe(CN)6]4- будет максимальным.
Рассмотрим реакцию получения нормального ферроцианида железа (III):
Чтобы получить плёнку Лэнгмюра-Блоджетт на основе этой реакции, необходимо чтобы один из реагентов был амфифильным и представлял собой нерастворимый монослой. Однако, выбор ПАВ, содержащих в своем составе железо, крайне ограничен. Одним из таких веществ является соль стеариновой кислоты FeSt3 и реакция образования пленки берлинской лазури может быть следующей:
Изучение изотерм сжатия монослоя FeSt3 на растворах желтой кровяной соли при pH = 3-5 позволяет сделать вывод о том, что это реакция не идет. Значения параметра А2,5 (площадь приходящаяся на молекулу при давлении 2,5 мН/м) на этих растворах практически совпадают со значениями на воде.
Другой способ получить БЛ в монослое взаимодействие с ПАВ в процессе образования берлинской лазури. При этом требования к ПАВ значительно ниже, чем в первом случае. Схема образования может быть следующей (ПАВ октадециламин):
При всех значениях pH параметр А2,5 увеличивается по сравнению с системой ОДА + H2O, что свидетельствует о прохождении первой стадии. Положительно заряженный монослой притягивает отрицательно заряженные комплексные ионы, монослой сжимается при уменьшении положительного заряда, но затем, при увеличении концентрации аниона в монослое, происходит перезарядка слоя - он становится отрицательно заряженным, и снова наблюдается его расширение.
При добавлении FeCl3 к системе ОДА-K4[Fe(CN)6] наблюдается еще большее увеличение площади, занимаемой одной молекулой. При реализации второй стадии предложенного механизма заряд монослоя должен уменьшаться, но этого не наблюдается. Причиной является рост кристаллов БЛ непосредственно в монослое.
Анализ полеченных данных позволил подобрать условия, способствующие получению пленок Лэнгмюра-Блоджетт с максимальным содержанием ферроцианидного аниона.
| Назад |
Оглавление |
Главная |